
Kan vi i framtiden få mediciner som bromsar åldrandet och gör oss friskare under våra sista år? Det låter som science fiction men behöver inte längre vara det. Runtom i världen forskas det numera intensivt på att förstå vad som driver åldrandet – från ett cellbiologiskt perspektiv.
Åldrandet börjar i cellernas inre. Med en allt högre levnadsstandard lever vi längre. Men åldrandet har ett pris i form av sjukdomar som cancer, diabetes typ II, Parkinson och Alzheimer.
Men tänk om vi kan senarelägga eller förhindra sjukdomarna genom att göra något åt åldrandet i sig? Att åldras utan att bli skröplig. Hoppet växer ju mer vi lär oss om vad som händer i cellens inre.
Det pågår ett komplicerat samspel mellan organellerna som är cellens egna inre organ. När vi åldras slutar organellerna att fungera, en efter en. Det innebär att den storstädning som ständigt pågår i cellen inte längre fungerar. För att hålla sig ung måste cellen göra sig av med proteiner som skadats, felveckats eller börjat klumpa ihop sig.
Mitokondrierna – kroppens kraftverk
– Det finns sju eller åtta organeller beroende på hur man räknar. Det är viktigt att de pratar med varandra och kan påverka varandra med sina funktioner. Men de är involverade i ett tusental olika processer. Vi fokuserar på de processer vi tror är viktigast för att förstå hur cellen åldras, säger Martin Ott, professor vid Institutionen för biokemi och biofysik på Stockholms universitet.
Vad Martin Ott och hans medarbetare funnit är att en av organellerna, mitokondriet, spelar en nyckelroll. Mitokondriet är cellens kraftverk. När detta utsätts för stress aktiverar det ett skyddsprogram som understöder cellens alla funktioner. Detsamma sker vid när cellen åldras – till en viss gräns. Bortom den blir den inre kommunikationen allt sämre.
Organellerna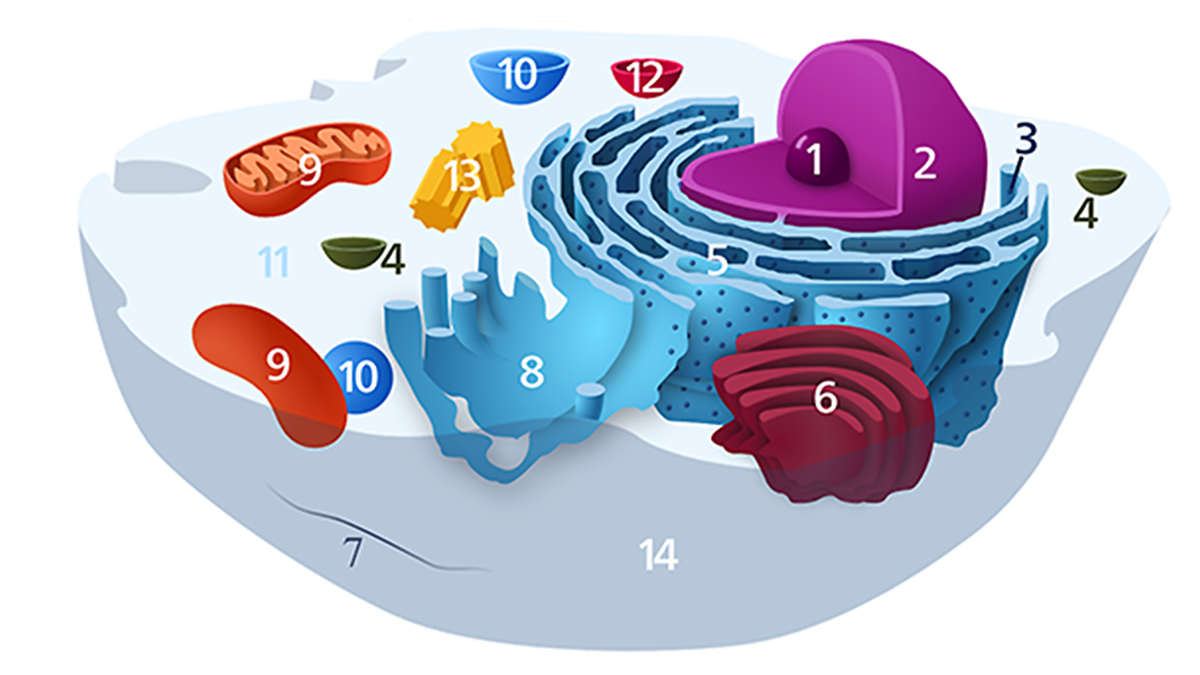
Organeller: (1) nukleol, (2) cellkärna, (3) ribosom, (4) vesikel, (5) grovt endoplasmatiskt retikulum (ER), (6) golgiapparaten, (7) cytoskelett, (8) slätt ER, (9) mitokondrie, (10) vakuol, (11) cytoplasma, (12) lysosom, (13) centriol och (14) cellmembran.
Den allra största organellen är själva cellkärnan, som innehåller arvsmassan i form av kromosomer. På 1930-talet upptäcktes att kromosomerna på sina ändar har skyddande ”hättor”, så kallade telomerer. Dessa ändar på DNA-trådarna är mycket sårbara. Med tiden förstod forskarna att telomererna förkortas i takt med att cellen åldras.
Telomererna – ändarna som skyddar dna
Utan telomerer skadas dna:et och celldelningen stoppas, varefter cellen dör. Många trodde att man nu hade hittat nyckeln som skulle lösa åldrandets gåta. Man föreställde sig till exempel att det skulle gå att mäta åldrandet genom att mäta längden på telomererna. I dag vet man åldrande inte är en följd av en, utan många komplicerade processer.
– Det finns test som visar hur långa telomererna är, och kopplingen mellan ålder och telomerlängd syns tydligt när man gör statistik på ett stort antal undersökta fall. Men i det enskilda fallet säger testvärdena bara att väldigt korta telomerer ger en större risk att dö i vissa sjukdomar som hjärtsjukdomar och infektionssjukdomar, säger telomerforskaren Marita Cohn vid Lunds universitet.

Under en period gästforskade hon hos Elizabeth Blackburn i San Francisco, en av dem som belönades med 2009 års Nobelpris i medicin för sin forskning om hur telomererna och ett enzym – telomeras – skyddar arvsmassan. Detta telomeras kan motverka att telomererna förkortas. Hos människa finns enzymet bara i vissa celler – framför allt i könsceller eftersom det är viktigt att cellerna hos nya individer får långa telomerer.
När Marita Cohn arbetade med Elizabeth Blackburn kunde hon visa att enzymet telomeras också finns i jästceller, något som är viktigt eftersom jäst är en vanlig modellorganism för att studera åldrande i cellen.
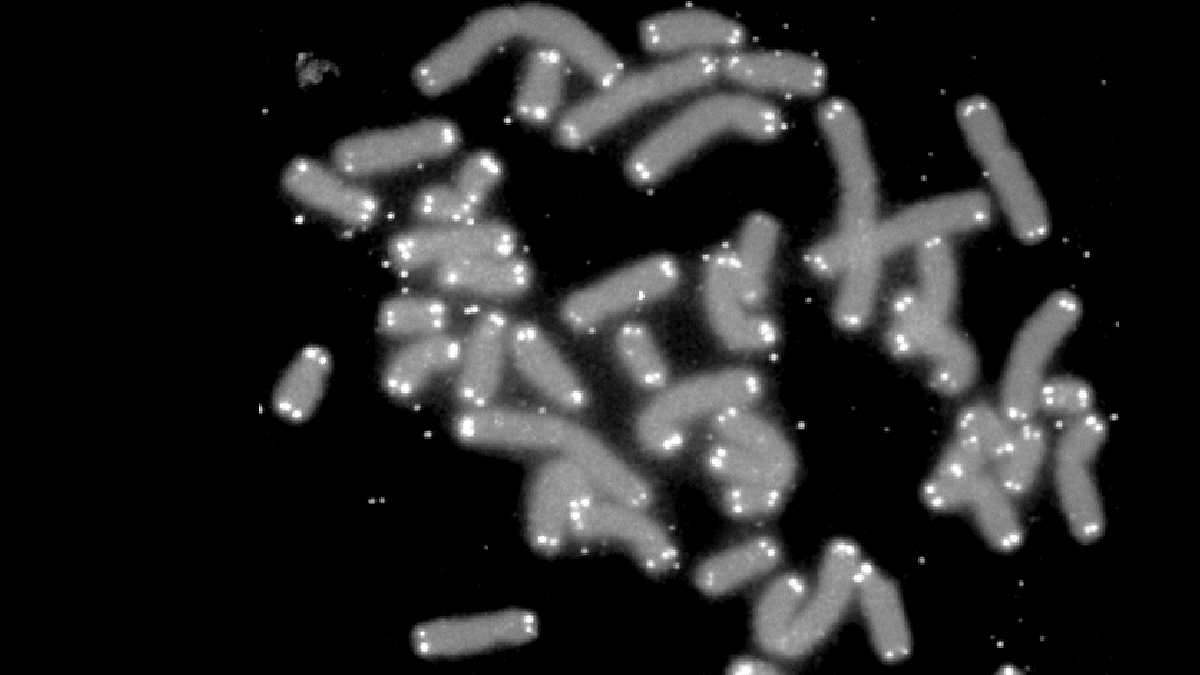
Telomeras aktivt vid cancer
– Idag vet man att telomeras finns hos många arter, säger Marita Cohn.
Det finns förstås alltid en koppling mellan forskningen kring åldrandet och alla de sjukdomar vi förknippar med just åldrande.
Cancer är ett tillstånd där cellerna delar sig ohämmat. I många cancerformer är enzymet telomeras extra aktivt och förlänger telomererna vilket i sin tur är kopplat till okontrollerad tillväxt. Det är som om cellerna fått evigt liv. Det har dock visat sig att det även finns andra sätt för tumörceller att bibehålla telomererna. 15 procent av alla cancerformer använder sig av en alternativ process kallad ALT (Alternative Lengthening of Telomeres), som Marita Cohn forskar kring idag.
Kosten påverkar telomererna
Vi kan påverka telomerernas längd genom att äta rätt kost, enligt forskning av nobelpristagaren Elizabeth Blackburns. Man bör undvika processad mat, rökt kött och livsmedelstillsatser. Det verkar också som om depressioner och negativt tänkande är skadligt medan meditation har en positiv inverkan.
Att cellerna i dag kan granskas så närgånget beror på ny teknik. Ett exempel på den saken är ett projekt lett av Christian Riedel på Karolinska Institutet, som studerar hur gener uttrycks för att bygga olika proteiner. En gen (DNA i cellkärnan) kodar för ett RNA (en bärarmolekyl i cytoplasma), som i sin tur översätts till ett protein (till exempel ett enzym, med olika funktioner i kroppen). På samma vis som de samlade generna kallas ”genom”, och de samlade proteinerna kallas ”proteom”, kallas översättningsledet med RNA-molekyler för ”transkriptom”. Genom att bearbeta den cellulära informationen hos transkriptomet i ett givet ögonblick, kan man registrera hur generna kommer till uttryck, det vill säga hur stora mängder det finns av varje typ RNA-molekyl. Med maskininlärning har Riedels forskargrupp tränat datorprogram att känna igen om ett transkriptom härrör från en ung eller gammal människa. Man har sedan använt sig av ett dataregister av 1300 substanser som kan påverka transkriptomet. – Med den här metoden kan vi identifiera substanser som ändrar transkriptomet i en riktning som är typisk för den yngre cellen, säger Christian Riedel. Vissa av dem är sedan tidigare kända för att ha en livsförlängande effekt, till exempel telomeraset. Men forskargruppen har också lyckats hitta substanser som man tidigare inte visste hade sådana egenskaper. Två av dem, monorden och tanespimycin, har redan testats på rundmaskar. Ytterligare några intressanta substanser står på tur att testas på detta sätt. – Ämnena förlängde maskarnas livslängd, och monorden förbättrade även deras hälsa. Dessa substanser är involverade i processer som hjälper cellens proteinmolekyler att behålla sin tredimensionella veckning, som i sin tur är avgörande för att ett protein ska kunna fullgöra sina uppgifter.Föryngringssubstanserna – jakt på ämnen som finns hos unga

Kalorier kontra livslängd
Hur olika proteiner samspelar är också tydligt när man tittar på iakttagelsen att ett lågt kaloriintag bromsar åldrandet, något som bekräftats i djurförsök på såväl apor som råttor.
Av naturliga skäl är det svårt att göra kontrollerade studier av detta på människa. Men det finns undersökningar gjorda i Norge och Danmark på hur befolkningen påverkades av 1:a och 2:a världskriget. Tillgången på föda var då begränsad, något som tycks ha bromsat åldrandet och uppkomsten av åldersrelaterade sjukdomar som cancer och diabetes typ II.
Ingen förstod hur en sänkning av kalorierna kunde påverka livslängden. Man visste att oxidanter, en grupp ämnen som anhopas i cellen, är giftiga och påskyndar åldrande och åldringssjukdomar. Men för några år sedan kunde en forskargrupp nu vid Chalmers tekniska högskola visa hur detta var relaterat till kosten.
– I cellerna finns enzymet peroxiredoxin som bryter ner väteperoxid och andra skadliga oxidanter i cellen. Men när cellerna åldras är enzymet inte längre lika effektivt. Genom att minska tillförseln av socker och proteiner till jästceller har vi visat att peroxiredoxinet inte sätts ur funktion, säger docent Mikael Molin, som leder forskargruppen vid Chalmers. Nyligen har man också funnit en koppling mellan peroxiredoxin och cellens dygnsrytm. Ämnesomsättningen ser olika ut vid olika tider på dygnet och styrs av biologiska klockor. För detta krävs vanligen någon form av ljusreceptorer. Jästsvamp som Molin använder sig av i sin forskning tycktes dock sakna en sådan mekanism – ända tills man upptäckte att peroxiredoxin på något ännu inte helt klarlagt sätt fungerar som en biologisk klocka. Det är ett intressant fynd; det är ju känt att störningar i dygnsrytmen både ökar risken för cancer och för förtidigt åldrande.Peroxiredoxinet – enzymet för kalorirestriktion
Text: Göran Frankel på uppdrag av forskning.se








