
Dna hålls ihop för att molekylens inre skyr vatten
Det är inte vätebindningar som håller ihop de båda strängarna i dna, som man hittills trott. Istället är det vatten som gör att DNA kan hållas samman när det inte kopieras eller repareras. Upptäckten, gjord av forskare vid Chalmers, ger ny grundläggande kunskap om dna, och kan bli användbar inom medicin och livsvetenskap.
Vår arvsmassa består av dna, som i sin utgörs av två strängar med sockermolekyler och fosfatgrupper. Mellan dessa sitter kvävebaser, alltså de atomföreningar som utgör organismens gener, med vätebindningar mellan sig. Hittills har den rådande uppfattningen varit att de båda strängarna hålls samman i en spiralformad “repstege” genom vätebindningar som sitter mellan de så kallade kvävebaserna på respektive sträng.
Forskare på Chalmers visar nu att dna:ts helixstruktur i själva verket upprätthålls främst av att molekylen har ett hydrofobt innehåll i en omgivning som normalt består mest av vatten. Miljön är alltså hydrofil, medan kvävebaserna i dna-molekylen är hydrofoba och därför stöter bort vatten som kommer i deras närhet. När hydrofoba enheter hamnar i en hydrofil miljö dras de till andra hydrofoba enheter för att minimera kontakt med vattnet.
Hydrofob = vattenavstötande
De vätebindningar som man hittills har betraktat som avgörande för att hålla ihop dna-helixen fungerar snarare som en kraft som sorterar basparen så att de länkas samman i rätt sekvens.
Upptäckten är avgörande för förståelsen för dna:s kontakt med omvärlden.
Dna-molekylen vilar i vatten
– Cellen vill skydda sitt dna, och alltså inte utsätta det för hydrofoba miljöer, där det finns andra, ibland skadliga molekyler, säger Bobo Feng, en av forskarna bakom studien. Men samtidigt måste cellens dna öppna sig då och då för att kunna användas.
– Vi menar att cellen har sitt dna i vattenlösning för det mesta, men så fort en cell vill göra något med sitt dna, som att läsa av det, kopiera det eller reparera fel på det, så utsätter den sitt dna för en hydrofob miljö.
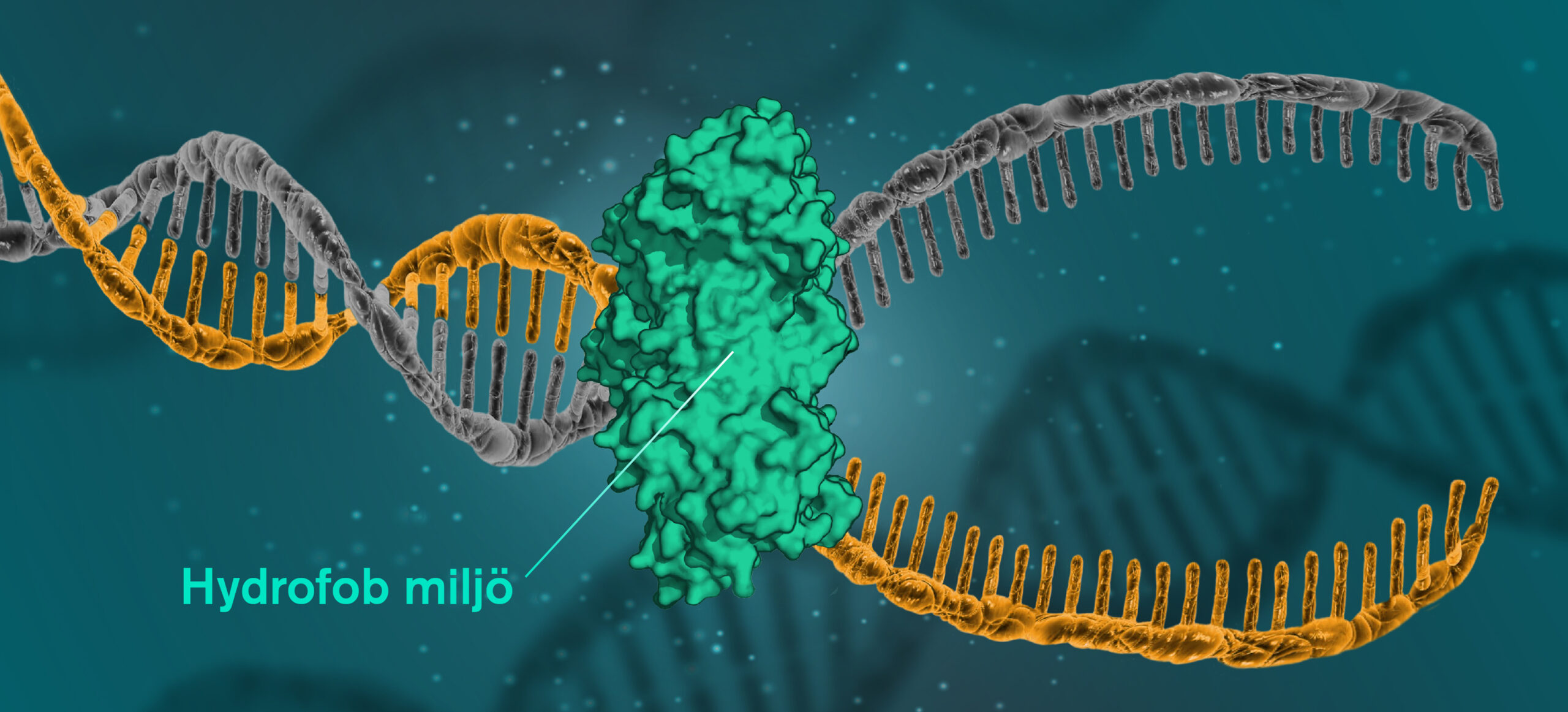
Vid reproduktion, till exempel, löses basparen från varandra och helixen öppnar sig. Därefter kan enzymer kopiera de båda strängarna av helixen och skapa nytt dna. Även när det gäller att reparera trasigt dna försätts den trasiga delen i en hydrofob miljö, för att sedan bytas ut. Det är då ett hjälpprotein som skapar den hydrofoba miljön. Denna typ av protein kan komma att bli nyckeln till att bekämpa en mängd allvarliga sjukdomar eftersom den är central i all dna-reparation.
Ger förståelse för hur dna repareras
Att förstå dessa proteiner kommer att ge många nya insikter om hur man skulle kunna bekämpa resistenta bakterier och även bota cancer. Bakterier reparerar sitt dna med ett protein som heter RecA. Forskarna tror att deras resultat kan bana väg för nya upptäcker om hur bakterier reparerar och återskapar sitt dna, och även metoder för att stoppa detta och därmed ta död på bakterierna.
I mänskliga celler finns proteinet Rad51 som reparerar dna och återskapar muterade dna-sekvenser, som annars skulle kunna orsaka cancer.
– För att förstå cancer behöver vi förstå hur dna repareras, och för att förstå hur dna repareras behöver vi förstå dna i sig, säger Bobo Feng. Hittills har vi inte förstått dna, eftersom vi har trott att det är vätebindningar som håller ihop det. Nu visar vi att det i stället är den hydrofoba kraften som ligger bakom. Vi säger dessutom att dna beter sig helt annorlunda om man placerar det i en hydrofob miljö. Detta kan hjälpa oss att förstå dna och hur det repareras. Ingen har tidigare placerat dna i en miljö som gränsar till det hydrofoba och studerat hur det beter sig, så det är inte konstigt att ingen har upptäckt detta förrän nu.
Chalmersforskarna har utvecklat en metod för att studera hur dna beter sig i en miljö som är mer hydrofob än normalt. De använde det hydrofoba lösningsmedlet polyetylenglykol och bytte stegvis ut dna:ts omgivning från den naturliga hydrofila miljön till en hydrofob miljö, för att se om det finns en gräns då dna-spiralen börjar tappa sin struktur, alltså då dna inte längre har anledning att hänga ihop eftersom miljön inte längre är hydrofil. När lösningen nådde en gräns mellan hydrofil och hydrofob, observerade forskarna att dna-molekylens karaktäristiska spiralform började säcka ihop. Vid en närmare undersökning visade det sig att när basparen lossnar från varandra (av yttre påverkan eller helt enkelt slumpmässiga rörelser) så bildas hål i strukturen så att vatten kan rusa in. Eftersom dna-molekylen “vill” hålla sitt inre torrt, pressas de över- och underliggande basparen ihop igen och trycker på så sätt ut vattnet. I en hydrofob miljö saknas detta vatten, så att hålet stannar kvar.
Vetenskaplig artikel:
Kontakt:
Bobo Feng, doktor i kemi och kemiteknik, Chalmers, bobo.feng@chalmers.se
Bengt Nordén, professor i kemi och kemiteknik, Chalmers, norden@chalmers.se




